- Главная
- Страница не найдена
Рекомендуемые товары
ЦенОТПАД
10094480
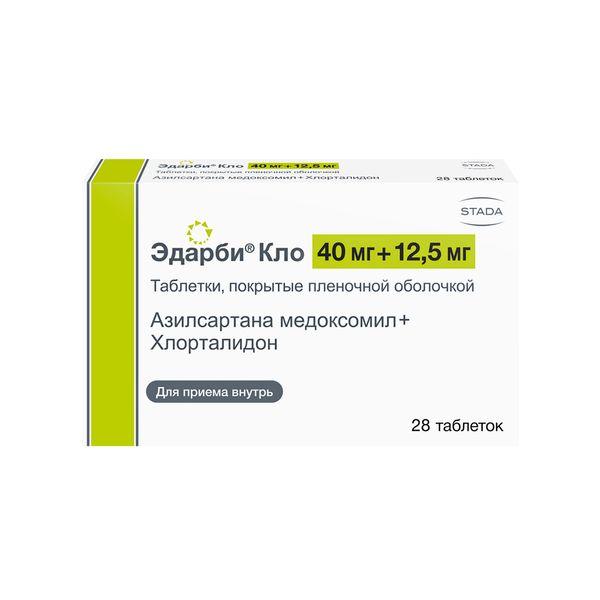
ЭДАРБИ КЛО ТАБЛ. П/ПЛЕН/ОБ. 40МГ+12,5МГ №28
По рецепту
Производитель:
ТАКЕДА АЙЛЭНД ЛИМИТЕД/ХЕМОФАРМ ООО
1105₽
1190₽
Стоп-Цена
-10%
7419
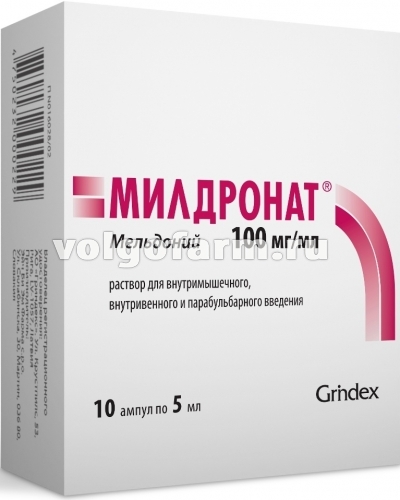
МИЛДРОНАТ Р-Р ДЛЯ В/В В/М И ПАРАБУЛЬБ. ВВЕД. 100МГ/МЛ АМП. 5МЛ №10
По рецепту
Производитель:
ЭЙЧ БИ ЭМ ФАРМА С.Р.О./ГРИНДЕКС АО
от 1305₽
1450₽
ЦенОТПАД
6529
АКТОВЕГИН ТАБЛ. П/О 200МГ №50
По рецепту
Производитель:
ТАКЕДА ФАРМАСЬЮТИКАЛС ООО/ТАКЕДА АВСТРИЯ ГМБХ
2020₽
2060₽
ЦенОТПАД
-5%
1049654
ВЕССЕЛ ДУЭ Ф КАПС. 250ЛЕ №60
По рецепту
Производитель:
КАТАЛЕНТ ИТАЛИ С.П.А./АЛЬФАСИГМА С.П.А.
от 3572₽
3760₽
ЦенОТПАД
-5%
8104
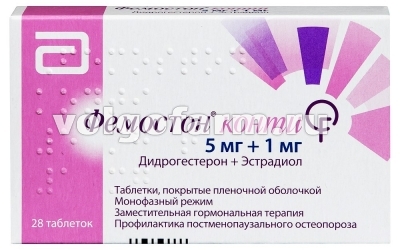
ФЕМОСТОН КОНТИ ТАБЛ. П/ПЛЕН/ОБ. 5МГ+1МГ №28
По рецепту
Производитель:
ЭББОТТ БИОЛОДЖИКАЛС Б.В.
от 1587₽
1670₽
ЦенОТПАД
35947
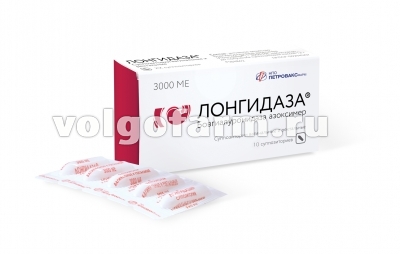
ЛОНГИДАЗА СУПП. ВАГ/РЕКТ. 3000МЕ №10
Производитель:
ПЕТРОВАКС ФАРМ НПО ООО
2660₽
2860₽
ЦенОТПАД
67149
КЛАЙРА НАБОР ТАБЛ. П/ПЛЕН/ОБ. 2МГ+2МГ, 3МГ+2МГ №28
По рецепту
Производитель:
БАЙЕР ВЕЙМАР ГМБХ И КО. КГ
1550₽
1595₽
ЦенОТПАД
41096
ДЖЕС ТАБЛ. П/ПЛЕН/ОБ. 3МГ+0,02МГ №28
По рецепту
Производитель:
БАЙЕР ВЕЙМАР ГМБХ И КО. КГ
1440₽
1540₽
ЦенОТПАД
8103
ФЕМОСТОН 1 ТАБЛ. П/ПЛЕН/ОБ. №28
По рецепту
Производитель:
ЭББОТТ БИОЛОДЖИКАЛС Б.В.
1590₽
1760₽
ЦенОТПАД
-7%
10011270
АЛФЛУТОП Р-Р Д/ИН. АМП. 2МЛ №10
По рецепту
Производитель:
РОМФАРМ КОМПАНИ С.Р.Л.
от 4566₽
4910₽
ЦенОТПАД
84065
ДЖЕС ПЛЮС ТАБЛ. П/ПЛЕН/ОБ. №28
По рецепту
Производитель:
БАЙЕР ВЕЙМАР ГМБХ И КО. КГ
1540₽
1610₽
ЦенОТПАД
84066
ЯРИНА ПЛЮС ТАБЛ. П/ПЛЕН/ОБ. 3МГ+0,03МГ+0,451МГ И 0,451МГ №28
По рецепту
Производитель:
БАЙЕР ВЕЙМАР ГИБХ И КО КГ/БАЙЕР АГ
1662₽
1770₽
ЦенОТПАД
1069800
КАНЕФРОН Н ТАБЛ. П/О №120
Производитель:
РОТТЕНДОРФ ФАРМА ГМБХ/ВИВЕЛХОФЕ ГМБХ
1465₽
1510₽
ЦенОТПАД
-5%
83461
ДИМИА ТАБЛ. П/ПЛЕН/ОБ. 3МГ+0,02МГ №28
По рецепту
Производитель:
ГЕДЕОН РИХТЕР ОАО
от 1245₽
1310₽
10023057
ЭЛИКВИС ТАБЛ. П/ПЛЕН/ОБ. 5МГ №60 ПФАЙЗЕР
По рецепту
Производитель:
ПФАЙЗЕР АЙРЛЕНД ФАРМАСЬЮТИКАЛС
от 2601₽